黃銅中銅質量分數的測定與分析
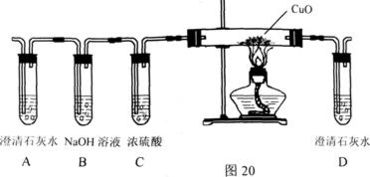
黃銅作為一種常見的銅鋅合金,因其良好的機械性能、耐腐蝕性和美觀的色澤,被廣泛應用于電器零件及日用品制造中。測定黃銅中銅的質量分數,對于控制產品質量、優化材料性能具有重要意義。本次實驗通過化學反應法,對一份黃銅樣品中的銅質量分數進行了測定。
實驗原理
黃銅中僅鋅能與稀硫酸發生置換反應,生成硫酸鋅和氫氣,而銅不與稀硫酸反應。反應方程式為:
Zn + H?SO? → ZnSO? + H?↑
通過測量反應前后總質量的變化,可以計算出反應生成氫氣的質量,進而推算出樣品中鋅的質量,最終求出銅的質量及其質量分數。
實驗數據與計算
已知:
- 黃銅樣品質量:10.0 g
- 加入稀硫酸質量:98.0 g
- 反應后燒杯中物質總質量:107.9 g
1. 計算生成氫氣的質量
根據質量守恒定律,反應前總質量 = 黃銅樣品質量 + 稀硫酸質量 = 10.0 g + 98.0 g = 108.0 g。
反應后總質量 = 107.9 g。
反應前后質量減少的部分即為逸出氫氣的質量。
氫氣質量 = 108.0 g - 107.9 g = 0.1 g。
2. 計算樣品中鋅的質量
設樣品中鋅的質量為 \( m{Zn} \)。
根據化學方程式:
Zn + H?SO? → ZnSO? + H?↑
65 g Zn 對應生成 2 g H?。
即:
\[ \frac{m{Zn}}{65} = \frac{0.1}{2} \]
解得:
\[ m_{Zn} = \frac{65 \times 0.1}{2} = 3.25 \text{ g} \]
3. 計算樣品中銅的質量及質量分數
銅的質量 = 樣品總質量 - 鋅的質量 = 10.0 g - 3.25 g = 6.75 g。
銅的質量分數 = \( \frac{6.75}{10.0} \times 100\% = 67.5\% \)。
結果與討論
本次測定得出,該黃銅樣品中銅的質量分數為67.5%,鋅的質量分數為32.5%。此組成屬于常見黃銅(如三七黃銅)的范圍,具有良好的綜合性能,適合用于制造對強度、延展性及耐腐蝕性有一定要求的日用品和電器零件。
在金屬日用品制造中,黃銅的應用十分廣泛。例如:
- 裝飾五金:如門把手、鎖具、燈具配件等,利用其金黃色的光澤和耐銹蝕特性。
- 廚具與餐具:部分高檔水龍頭、酒器、裝飾性餐具采用黃銅制造,常進行表面鍍鉻或鎳處理以增強耐用性和衛生性。
- 樂器與工藝品:如薩克斯管、號等管樂器,以及雕塑、獎牌等工藝品,利用其優異的聲學性能和易加工性。
- 電器零件:如插頭、插座觸點、散熱器等,利用其良好的導電性和導熱性。
實驗意義與注意事項
本實驗方法簡單、原理清晰,通過基礎的化學定量分析即可獲得合金組成。在實際工業生產中,控制黃銅中銅鋅比例是調整其硬度、強度、塑性及耐腐蝕性的關鍵。例如,含銅量較高的黃銅(如65%-70%)更柔軟、延展性更好,適合冷加工;而含鋅量增高則會提高強度和硬度,但脆性也可能增加。
需要注意的是,實驗中假設稀硫酸足量且反應完全,所有氫氣均逸出并被準確計量。實際操作中需確保反應完全,并考慮環境因素對稱量的影響,以提高測定精度。黃銅中可能含有少量其他元素(如鉛、錫、鋁等),對于更高精度的成分分析,可能需要借助光譜分析等儀器方法。
綜上,化學分析法為理解合金組成提供了一種直觀的手段,而黃銅作為一種經典合金材料,其成分與性能的關聯性,持續支撐著它在日用品制造及工業領域中的重要地位。
如若轉載,請注明出處:http://www.lengchucun.cn/product/69.html
更新時間:2026-05-10 04:10:59








